American College of Obstetricians and Gynecologists. Novel coronavirus 2019 (COVID-19) [Internet] Washington, DC, American College of Obstetricians and Gynecologists, 2020a;[cited 2020 Sep 15]. Available from:, https://www.acog.org/clinical/clinical-guidance/practice-advisory/articles/2020/03/novel-coronavirus-2019
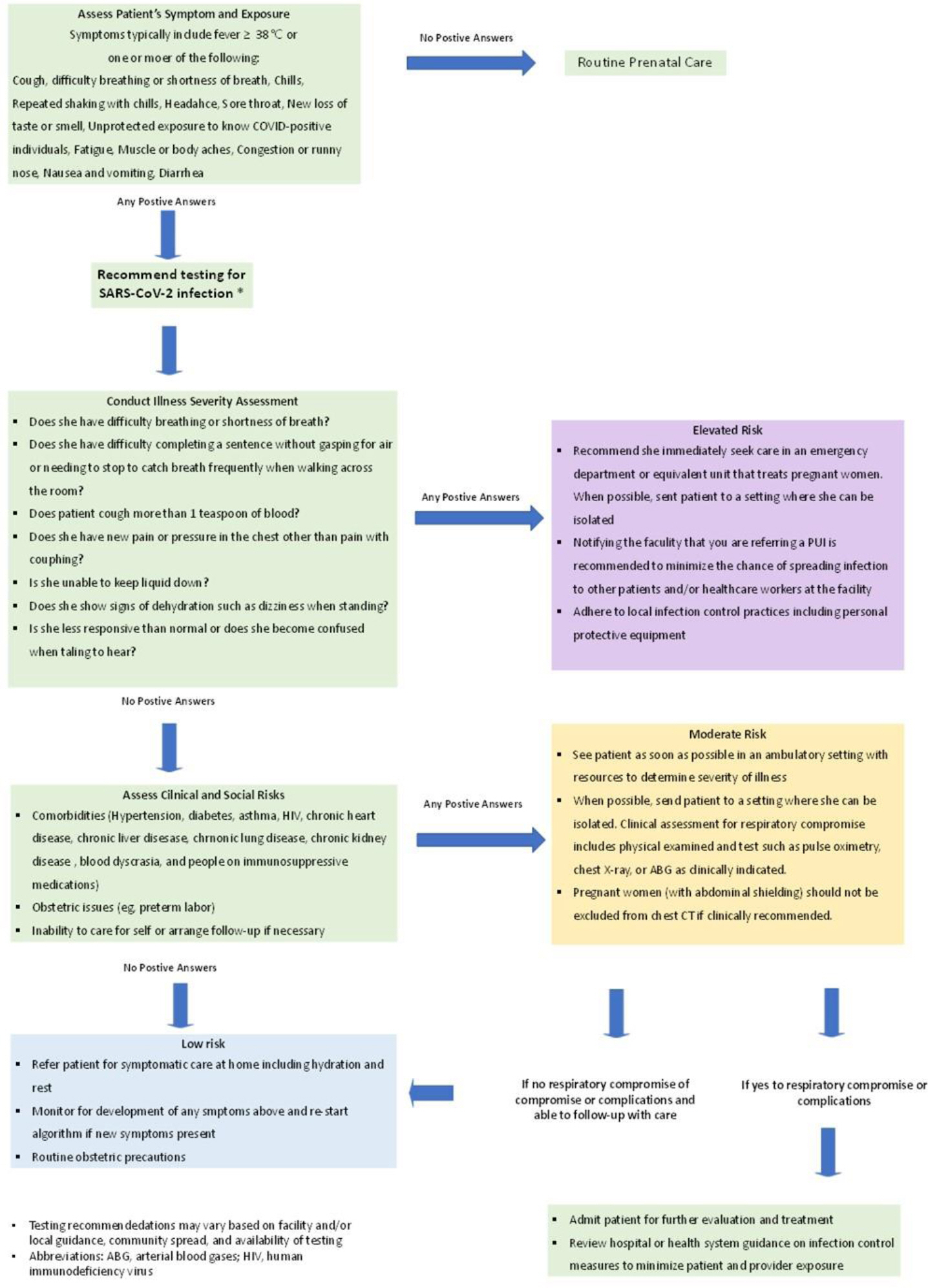
American College of Obstetricians and Gynecologists. Outpatient assessment and management for pregnant women with suspected or confirmed novel coronavirus (COVID-19) [Internet] Washington, DC, American College of Obstetricians and Gynecologists, 2020b;[cited 2020 Sep 15]. Available from:, https://www.acog.org/-/media/project/acog/acogorg/files/pdfs/clinical-guidance/practice-advisory/covid-19-algorithm.pdf
American College of Obstetricians and Gynecologists. Vaccinating pregnant and lactating patients against COVID-19 [Internet] Washington, DC, American College of Obstetricians and Gynecologists, 2021;[cited 2021 Jan 4]. Available from:, https://www.acog.org/clinical/clinical-guidance/practice-advisory/articles/2020/12/vaccinating-pregnant-and-lactating-patients-against-covid-19
Centers for Disease Control and Prevention. Evaluation and management considerations for neonates at risk for COVID-19 [Internet] Atlanta (GA), Centers for Disease Control and Prevention, 2020;[cited 2020 Sep 15]. Available from:, https://www.cdc.gov/coronavirus/2019-ncov/hcp/caring-for-newborns.html
Centers for Disease Control and Prevention. CDC COVID data tracker. United States COVID-19 cases and deaths by state [Internet] Atlanta (GA), Centers for Disease Control and Prevention, 2021a;[cited 2021 Jan 4]. Available from:, https://covid.cdc.gov/covid-data-tracker/#cases_casesper100klast7days
Centers for Disease Control and Prevention. CDC COVID data tracker. Data on COVID-19 during pregnancy: severity of maternal illness [Internet] Atlanta (GA), Centers for Disease Control and Prevention, 2021b;[cited 2021 Jan 4]. Available from:, https://covid.cdc.gov/covid-data-tracker/#pregnant-population
Centers for Disease Control and Prevention. The Advisory Committee on Immunization Practices' Updated Interim Recommendation for Allocation of COVID-19 Vaccine — United States, December 2020 [Internet] Atlanta (GA), Centers for Disease Control and Prevention, 2021c;[cited 2021 Jan 4]. Available from:, https://www.cdc.gov/mmwr/volumes/69/wr/mm695152e2.htm?s_cid=mm695152e2_w
Central Disease Control Headquarters, Central Disaster Management Headquarters. Coronavirus-19 Response Guidelines (Local Government Use). 9-4 edition [Internet] Cheongju (Korea), Central Disease Control Headquarters, Central Disaster Management Headquarters, 2020;[cited 2020 Dec 15]. Available from:, http://www.gidcc.or.kr/epvbr/%EC%BD%94%EB%A1%9C%EB%82%98%EB%B0%94%EC%9D%B4%EB%9F%AC%EC%8A%A4%EA%B0%90%EC%97%BC%EC%A6%9D-19covid-19/
Central Disease Control Headquarters, Central Disaster Management Headquarters. COVID-19 patient status [Internet] Cheongju (Korea), Central Disease Control Headquarters, Central Disaster Management Headquarters, 2021;[cited 2021 Jan 4]. Available from:, http://ncov.mohw.go.kr/
Chen H, Guo J, Whang C, Fan L, Yu X, Zhang W, et al. Clinical characteristics and intrauterine vertical transmission potential of COVID-19 infection in pregnant women: a retrospective review of medical records. Lancet 2020;395:809-15.


Gustavson K, Ask H, Ystrom E, Stoltenberg C, Lipkin WI, Suren P, et al. Maternal fever during pregnancy and offspiring attention deficit hyperactivity disorder. Sci Rep 2019;9:9519.


Huntley BJF, Suntely ES, Mascio DD, Chen T, Berghella V, Chauhan P. Rates of maternal and perinatal mortality and vertical transmission in pregnancies complicated by severe acute respiratory syndrome coronavirus 2 (SARS-Co-V-2) infection. Obstet Gynecol 2020;136:303-12.


Liu Y, Chen H, Tang K, Guo Y. Clinical manifestations and outcomes of SARS-CoV-2 infection during pregnancy. J Infect 2020 Mar 4;[Epub]., https://doi.org/10.1016/j.jinf.2020.02.028

National Institutes of Health. COVID-19 treatment guideline [Internet] Bethesda (MD), National Institutes of Health, 2020;[cited 2020 Sep 15]. Available from:, https://www.covid19treatmentguidelines.nih.gov/immune-based-therapy/immunomodulators/corticosteroids/
Poon LC, Abramowicz JS, Dall'Asta A, Sande R, ter Haar G, Marsal K, et al. ISUOG Safety Committee Position Statement on safe performance of obstetric and gynecological scans and equipment cleaning in context of COVID-19. Ultrasound Obstet Gynecol 2020a;55:709-12.


Poon LC, Yang H, Dumont S, Lee JCS, Copel JA, Danneels L, et al. ISUOG Interim Guidance on coronavirus disease 2019 (COVID-19) during pregnancy and puerperium: information for healthcare professionals - an update. Ultrasound Obstet Gynecol 2020b;55:848-62.


RECOVERY Collaborative Group. Horby P, Lim WS, Emberson JR, Mafham M, Bell JL, et al. Dexamethasone in hospitalized patients with Covid-19-Preliminary report. N Engl J Med 2020;NEJMoa2021436.
Royal College of Obstetrics and Gynaecologists. Coronavirus (COVID-19) infection in pregnancy [Internet] London, Royal College of Obstetricians and Gynaecologists, 2020a;[cited 2020 Sep 15]. Available from:, https://www.rcog.org.uk/globalassets/documents/guidelines/2020-07-24-coronavirus-covid-19-infection-in-pregnancy.pdf
Royal College of Obstetrics and Gynaecologists. Guidance for maternal medicine services in the evolving coronavirus (COVID-19) pandemic [Internet] London, Royal College of Obstetricians and Gynaecologists, 2020b;[cited 2020 Sep 15]. Available from:, https://www.rcog.org.uk/globalassets/documents/guidelines/2020-07-10-guidance-for-maternal-medicine.pdf
Society for Maternal Fetal Medicine. Coronavirus (COVID-19) and pregnancy: what maternal-fetal medicine sub-specialists need to know [Internet] Washington, DC, Society for Maternal Fetal Medicine, 2020;[cited 2020 Sep 15]. Available from:, https://www.smfm.org/covidclinical
Sutton D, Fuchas K, D'Alton M, Goffman D. Universal screening for SARS-CoV-2 in Women Admitted for delivery. N Engl J Med 2020;382:2163-4.


World Health Organization. WHO coronavirus disease 2019 (COVID-19) situation report 46 [Internet] Geneva (Switzerland), World Health Organization, 2020;[cited 2020 Sep 15]. Available from:, http://www.who.int/docs/default-source/coronavirus/situation-report/20200306-sitrep-46-covid-19.pdf?sfvrsn=96b04adf_2
Zaigham M, Andersson O. Maternal and perinatal outcomes with COVID-19: a systematic review of 108 pregnancies. Acta Obstet Gynecol Scand 2020;99:823-9.